细菌毒素可能引发多发性硬化发作和复发
根据威尔康奈尔医学院和纽约长老会的一组研究人员领导的一项新研究,一种特定的产生毒素的肠道细菌可能是引发多发性硬化症(MS)发作和持续疾病活动的原因。
该团队正在与康奈尔大学伊萨卡校区以及加州大学圣地亚哥分校的调查人员合作;加州大学戴维斯分校和匹兹堡大学;并与洛克菲勒大学的科学家有着长期的合作。
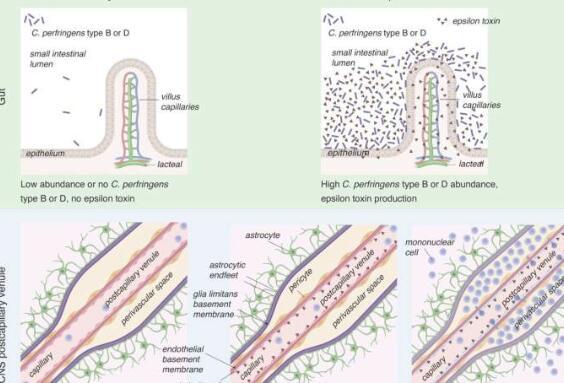
这项工作发表在《临床研究杂志》上,在MS患者的肠道微生物组中发现了产生ε毒素的产气荚膜梭菌异常高的丰度。该研究继续表明,在MS的临床前模型中,ε毒素打开大脑的血管,使炎症细胞进入中枢神经系统并引起MS特有的脱髓鞘。
MS 是一种致残的中枢神经系统疾病,通常在成年早期发病,仅在美国就影响近 1 万人。在病程早期,MS 的特征是发作性复发和神经系统症状缓解,包括视力丧失、虚弱和失衡。在病程后期,尽管治疗取得了许多进展,但大约 40% 的患病个体往往会进展 MS。
“MS有很多谜团,”共同资深作者Timothy Vartanian博士说,他是威尔康奈尔医学Feil家庭大脑和心灵研究所的神经科学教授。“为什么有些人会得MS,而另一些人不会,尽管遗传相似或相同?是什么导致了复发和缓解的发作性质?中枢神经系统是如何靶向的,为什么是髓磷脂?产气荚膜梭菌和ε毒素可以解释其中的许多奥秘。
MS在遗传易感个体中发生需要环境触发因素,MS患者中产ε毒素产气荚膜梭菌的丰度表明它可能是罪魁祸首。产气荚膜梭菌产ε毒素菌株生活在小肠中,并且仅在细菌处于生长期时短暂产生ε毒素,符合MS的复发缓解性质。也许最值得注意的是,ε毒素专门针对脑血管和髓磷脂,为其作用提供了明确的机制。
尽管越来越多的证据表明产气荚膜梭菌产生ε毒素的菌株可能是MS的相关环境病原体,但对该疾病患者肠道微生物组的现代研究未能检测到这些菌株。在目前的研究中,Vartanian实验室神经科学研究助理教授Yinghua Ma与大脑与心灵研究所的共同主要作者David Sanneno和Jennifer Linden一起领导了工作,表明更敏感的技术很容易在MS肠道微生物组中检测到这些菌株。
“以前的研究将使用一种方法,你可以看到那里的细菌物种,但你实际上看不到毒素或物种的一些功能更相关的部分,”共同资深作者Christopher Mason说,他是生理学和生物物理学教授,威尔康奈尔医学世界定量预测计划的联合主任。
使用高度灵敏的DNA检测技术,Ma发现MS患者比健康对照组更有可能在小肠中携带产生ε毒素的产气荚膜梭菌。
“该团队带来了现代分子生物学的全部武器,以解决发病机制和多发性硬化症的可能驱动因素的问题,”梅森说,他也是威尔康奈尔医学大脑与心灵研究所的神经科学教授。在确定了这种相关性后,研究人员测试了毒素是否会导致这种疾病。
为此,他们转向MS的标准小鼠模型,其中动物易发生自身免疫,但MS样疾病仅在小鼠也被给予百日咳毒素时才会发生。Ma用ε毒素代替百日咳毒素,动物患上了一种与以前的模型更相似的疾病。
“在MS小鼠模型中,epsilon毒素可以取代百日咳毒素的发现非常令人兴奋,”共同作者Gregory F. Sonnenberg说,他是Henry R. Erle,医学博士 - 罗伯茨家族医学副教授,威尔康奈尔医学院Jill Roberts炎症性肠病研究所的成员。
“它不仅推进了一个更相关的MS研究模型,而且批判性地定义了一种新的微生物衍生决定因素,该决定因素引起中枢神经系统免疫特权的崩溃,从而引发脱髓鞘疾病。
“Epsilon 毒素在 MS 病变形成的最早阶段起作用,”Vartanian 说,他也是威尔康奈尔医学院神经病学系多发性硬化症和神经免疫学部门的负责人,也是纽约长老会/威尔康奈尔医学中心的神经学家。“中和ε毒素的治疗可能会阻止我们患者的新疾病活动,比目前抑制或调节免疫系统的治疗方式更有效。
“在短期内,我们受到紧迫感的驱使,为MS患者提供更有效,更安全的治疗方法,”Vartanian说。
免责声明:本文由用户上传,与本网站立场无关。财经信息仅供读者参考,并不构成投资建议。投资者据此操作,风险自担。 如有侵权请联系删除!
-
【半五五分是什么生肖,揭晓词语落实释义】经过权威解读分析,落实打一生肖精准答案。一、权威答案:“半五五分...浏览全文>>
-
【穷言杂语是什么生肖,最佳释义解释指导】经过权威解读分析,落实打一生肖精准答案。一、权威答案:“穷言杂语...浏览全文>>
-
【舍近求远是什么生肖,揭晓词语释义解释】经过权威解读分析,落实打一生肖精准答案。一、权威答案:“舍近求远...浏览全文>>
-
【简单又搞笑的集体游戏】在聚会、团建或者班级活动中,选择一款简单又搞笑的集体游戏,不仅能活跃气氛,还能...浏览全文>>
-
【简单又带动气氛的舞蹈有什么】在聚会、派对或家庭活动中,选择一款简单又能够带动气氛的舞蹈,不仅能活跃现...浏览全文>>
-
【简单又充满气质的昵称】在社交平台、游戏、论坛等场合,一个合适的昵称不仅能让人印象深刻,还能体现出个人...浏览全文>>
-
【简单有哲理的句子】在日常生活中,我们常常会被一些看似简单却意味深长的话语所打动。这些句子虽然简短,却...浏览全文>>
-
【简单有意义的网名】在当今网络社交日益频繁的时代,一个合适的网名不仅能够体现个人风格,还能让人更容易记...浏览全文>>
-
【简单有效消灭蚂蚁的方法】蚂蚁虽然体型小,但它们的破坏力不容小觑。无论是厨房、客厅还是阳台,一旦出现蚂...浏览全文>>
-
【简单有效的瘦脸操】想要拥有更紧致、立体的面部轮廓,除了良好的饮食和作息习惯外,适当的瘦脸操也是不可忽...浏览全文>>
